时间:2021-04-12 11:55:07 点击:次

一、SARS-CoV-2病原学简介
新冠病毒(SARS-CoV-2)属于冠状病毒。冠状病毒属于套式病毒目、冠状病毒科、冠状病毒亚科,是自然界广泛存在的一大类病毒家族。从人冠状病毒而言,目前发现可感染人类的冠状病毒共有7种,分别是HCoV-229E、HCoV-OC43、HCoV-HKU1、SARS-CoV、MERS-CoV和新型冠状病毒;哺乳动物冠状病毒:可感染猪、犬、猫、鼠、牛、马等多种动物;禽冠状病毒:可引起鸡、火鸡、麻雀、鸭、鹅、鸽子等。
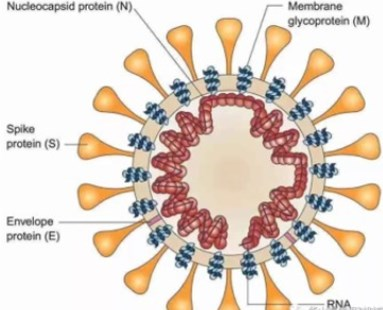
冠状病毒最早被发现是在20世纪30年代(1937年),从家禽身上分离到冠状病毒,即是鸡传染性支气管炎。随后于1986年,第一次从人身上发现了冠状病毒。至此以后,从兽医、人医、医学界、生物技术界都非常关注冠状病毒。从电镜下观察该病毒,形态似皇冠,故称之为冠状病毒,目前流行的主要是冠状病毒科和冠状病毒亚科的病毒。冠状病毒分为α、β、γ、δ四个属,其中α、β感染哺乳动物和人。如新冠病毒、HCoV-OC43属于β病毒, HCoV-229E属于α病毒(主要引起普通流感)。
另,猪的流行性腹泻、猪传染性胃肠炎属于α病毒属。犬、猫属大部分是α病毒属(部分蝙蝠属于β病毒属,有人称本次新冠病毒是由蝙蝠传染过来的,也情有可原)。γ、δ病毒属主要感染禽类,如鸡传染性支气管炎是γ属的,它主要是感染鸡、野鸡、火鸡等。δ属主要在雁、鸽子较为常见。总体上讲,γ、δ两个属与人的交叉、交接比较少,α、β属与人、哺乳动物交接比较多。冠状病毒传播途径主要是通过空气传播,也经过粪-口传播。一般情况下,呼吸道等疾病多是通过粪口传播和呼吸道传播。
关于人的新冠病毒SARS-CoV-2,它是导致目前COVID-19大流行的病原体,是一种新型的β冠状病毒。SARS-CoV-2可以引起严重肺炎。众所周知,2004年,在中国华南地区发生了SARS(β病毒属),目前能感染人的冠状病毒主要有7类,新冠病毒则属于第7类。前两类SARS、 HCoV-229E、HCoV-OC43都是引起流感的。另外,中东呼吸综合征(MARS)是高致病性病毒,死亡率达20%~30%。SARS的死亡率相对较低,为9%~10%。现流行的新冠病毒,死亡率最高为3%~4%,一般情况下不超过1%。新冠病毒基因组编码共29个蛋白,其中结构蛋白有4种,分别为:刺突蛋白(S蛋白)、 核衣壳蛋白(N蛋白)、 膜蛋白(M蛋白)和包膜蛋白(E蛋白)。
通过对新冠病毒进行冷冻电子断层扫描(cryo-ET)和子断层扫描图平均化(STA)3D解析发现,S蛋白通过识别细胞膜上的受体位点进行接触,然后突破细胞膜进入细胞,利用自身的基因组先合成RNA聚合酶,然后再利用这个RNA聚合酶反转录形成副链,以副链为模板一次性合成mRNA和病毒基因组。
因为冠状病毒是正链病毒,不经过修饰,直接复制形成基因组,所以冠状病毒容易发生基因变异和漂移。基因的多次变异和漂移导致基因组发生改变,诱导的蛋白和表达的核酸也因此改变,病毒的免疫原性和抗原性也随之改变,导致冠状病毒的种属多,感染面广。
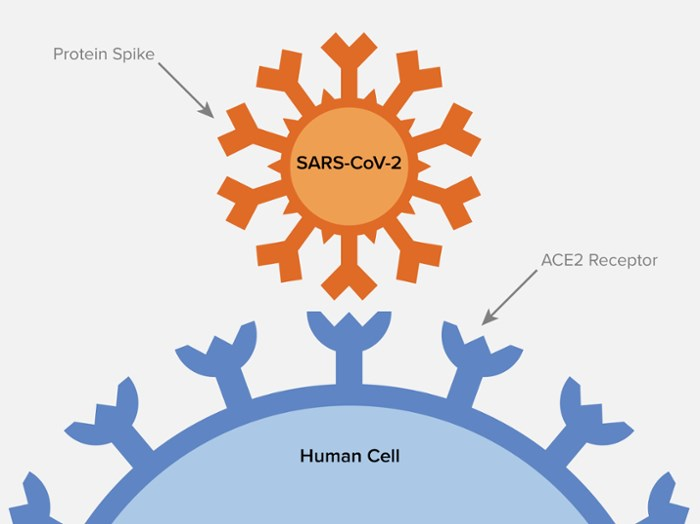
S蛋白通过受体结合域(RBD)与细胞表面受体血管紧张素转化酶2(ACE2)结合,从而入侵细胞。
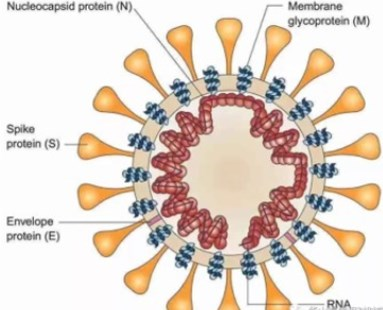
冷冻电子断层扫描(cryo-ET)和子断层扫描图平均化(STA)3D解析
二、SARS-CoV-2病毒检测方法
新型冠状病毒首先感染呼吸道,所以首先应对呼吸道进行检测。目前人医建立的检测程序较为规范和完善。首先讲一下核酸检测。在选择靶基因时,选择开放阅读框1ab(oopen reading frame lab, ORF1ab)、N蛋白、E蛋白和M蛋白其中任何一种蛋白基因,都能够检测到冠状病毒。为了能够保证检测到新型冠状病毒,通常进行双靶标设计,首先选择突变较大的S蛋白作为其中一个靶基因进行探针标记,另外再选择任一个蛋白(N蛋白或M蛋白)作为靶基因进行探针标记,这样双靶标同时检测阳性时,可以区分新型冠状病毒与其他冠状病毒。
如果只有N蛋白或者M蛋白对应靶标检测阳性时,有可能是其他的冠状病毒。目前,核酸检测试剂盒所采用的检测方法主要有实时荧光PCR法、恒温扩增法、联合探针锚定聚合测序法、杂交捕获免疫荧光法、RNA捕获探针法、RNA恒温扩增捕获—金探针层析法、双扩增法以及基于下一代测序技术( next-genera-tion sequencing,NGS) 等。目前常用实时荧光PCR法进行检测,用时短,结果可靠。
此外,对于核酸检测注意事项,要求是非常严格的,从样本采集、样本转运、样本接收、核酸提取以及PCR扩增及报告的解读,到生物医疗垃圾的处理,都有严格的程序规定和相关要求。

关于SARS-CoV-2抗体检测
有人问,为何诊断SARS-Co-2时既要检测核酸又要检测抗体。因为有些健康携带者或者隐性感染者,虽然未出现临床症状,但血液中带有抗体。抗体主要是IgM和IgG。一般来说,Ig产生较快,通常在感染后7~10天产生,而IgG通常在感染后2~3周产生。有些自然强毒感染时,会损伤淋巴细胞,因此,在感染后3周可能IgG含量仍然很低。
SARS-CoV-2抗体检测要按照国家规定进行,包括《新型冠状病毒肺炎诊疗方案(试行第八版)>将“SARS-CoV-2 特异性抗体Ig阳性”作为疑似病例诊断依据之一,并指出“SARS-CoV-2特异性抗体IgM和IgG在发病1周内阳性率较低,一般不单独以血清学检测作为诊断依据,需结合流行病学史、临床表现和基础疾病等情况进行综合判断”,强调动态观察抗体水平变化。因此,核酸检测仍是判断SARS CoV-2感染的金标准,抗体检测可用于核酸检测阴性疑似病例的补充检测,或在疑似病例诊断中与核酸检测联合应用,但不能代替核酸检测单独作为 SARS-CoV-2感染者确诊与否的依据,亦不适用于一般人群的筛查。同上,抗体检测我们也有注意事项及相关要求,希望大家重视。
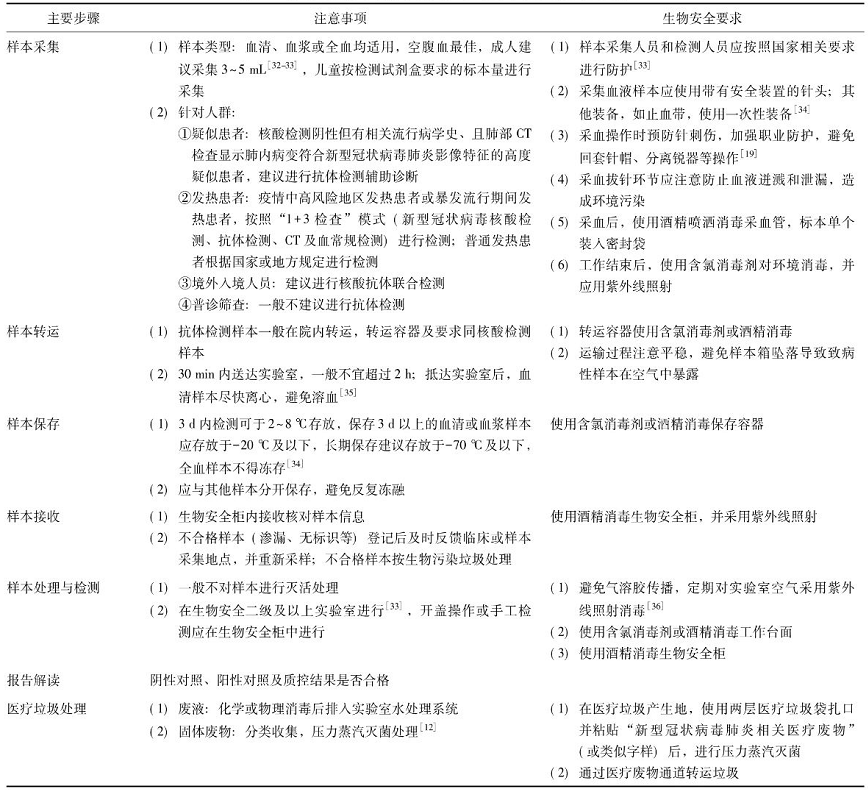
三、SARS-CoV-2生物安全要求
同时根据不同防护级别,对人体安全防护要求明确,包括防护服、手套、医用防护口罩等防护用品的规范使用。
采集的临床标本应尽量采集病例发病早期的呼吸道标本(尤其是下呼吸道标本)、和发病7天内急性血清以及发病后第3-4周的恢复血清:.
——上呼吸道标本可采集咽拭子、鼻咽拭子等
——下呼吸道标本包括深咳痰液、呼吸道吸取物、支气管或肺泡灌洗液、肺组织活检标本等
——眼结膜拭子、粪便标本、抗凝血和血清标本等
——死亡病例可按照规定采集尸体标本,或呼吸道灌洗液或经皮穿刺采集肺组织标本
——其他需要进一步筛查检测的环境或生物材料
所有标本采集后,必须装入密封的螺口塑料离心管中,拧紧瓶盖后再运到实验室,运输前尽可能对容器外壁做好消毒。
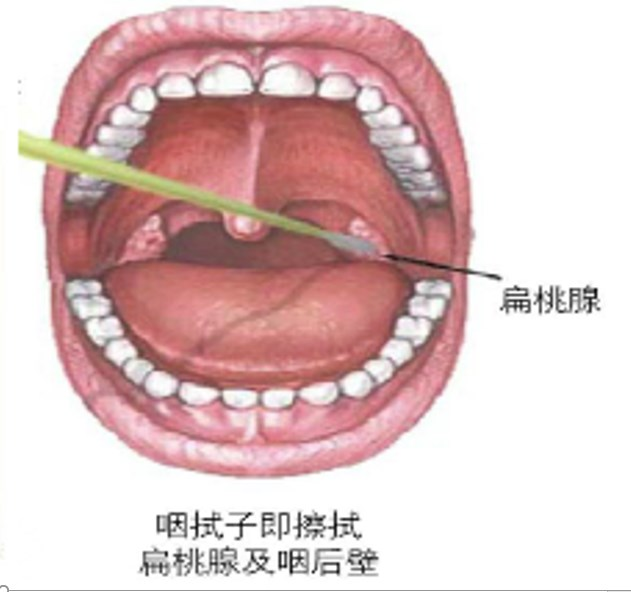
(1)口咽拭子采集方法:用1根聚丙烯纤维头的塑料杆拭子同时擦拭双侧咽扁桃体及咽后壁,将拭子头浸入含3ml病毒保存液的管中,尾部弃去,旋紧管盖。
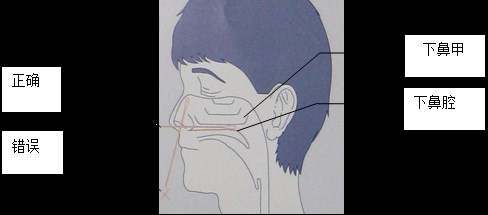
(2)鼻咽拭子采集方法:将1根聚丙烯纤维头的塑料杆拭子轻轻插入鼻道内鼻腭处,停留片刻后缓慢转动退出。取另一根聚丙烯纤维头的塑料杆拭子以同样的方法采集另一侧鼻孔。上述两根拭子浸入同一含3ml采样液的管中,尾部弃去,旋紧管盖。
(3)动物标本采集方法:参照人口咽拭子采集方法。
(4)环境标本采集方法:用3cm×6cm大小纱布用生理盐水或PBS浸湿拧干后最大程度的擦拭待检测物品表面及包装袋内外侧;粪污等液体、半固体样本搅匀后采集3~5g;粉状固体样本混置于样品袋中,送实验室检测。
从操作和规范角度看,人医比兽医在这一块比要求更为严格的。建议今后采集动物及其相关样本,如猪传染性胃肠炎、猪流行性腹泻需要采集肛门试纸、鼻腔试纸、唾液的可以参照人医的方法。另外,要重视新冠病毒的环境检测,如包装、包装台、冷藏仓等。目前非洲猪瘟在我国形成了一定的污染面,因为ASF主要是通过粪-口传播,某种程度上说环境污染是造成ASF传播的重要因素。个人考虑,如果将来要控制或净化ASF,除了动物引种严格要求外,要格外重视环境因素。
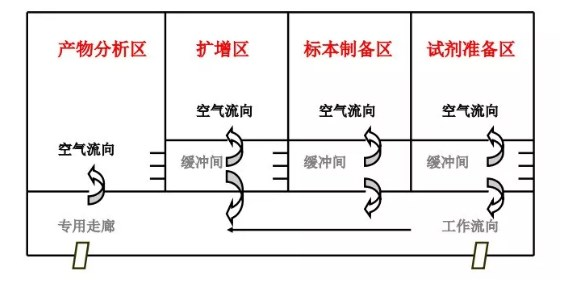
在物理空间上,试剂准备区、样品制备区、扩增区和扩增产物分析区是完全相互独立的并设有专用走廊,各区域无论是在空闲还是在使用中始终处于完全的分隔状态,不能有空气的直接相通,每个功能区都设置一个独立的缓冲室,工作区与缓冲间安装连锁装置。
设有高效过滤新风系统、采用全送全排的气流组织形式,通过严格控制送、排风的比例,调整各区域的气压,使整个PCR实验室避免气溶胶的污染。PCR实验室缓冲室内设置正压,防止室内空气外流,室外空气内流。
各区域有单向实验流程、物流、人流和气流,形成单向过程的防护屏障,避免实验干扰和实验过程中核酸气溶胶污染的假性结果。
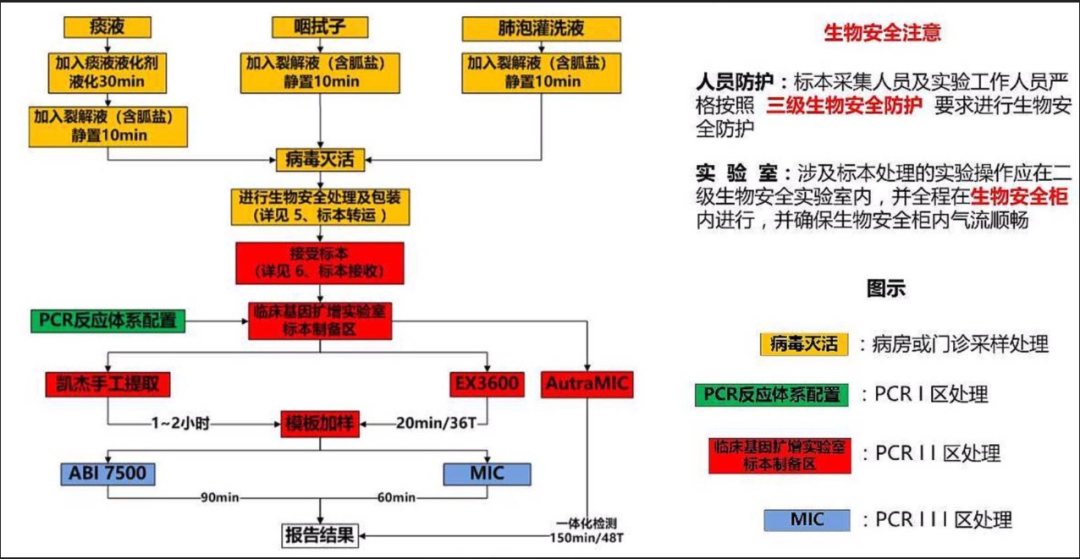
实验室清洁消毒
按照《医疗机构消毒技术规范》和疫情期间相关规定,做好清洁消毒工作。
环境及物表:用1000mg/L含氯消毒剂进行消毒,每天至少4次。不耐腐蚀的物表可用75%的酒精进行消毒。如有肉眼可见污染物时可用一次性吸水材料(如纱布、抹布等)沾取5000~10000mg/L 的含氯消毒液小心移除。如遇体液及血液污染时,立即用5000mg/L的含氯消毒剂消毒处理。
•空气消毒:用紫外线灯或空气消毒机消毒。
• 实验室物品表面(包括鼠标、读卡器等)、开关、门把手每天用500mg/L的含氯消毒剂擦拭消毒2次。
• 地面用500mg/L的含氯消毒剂喷洒或擦拭至少2次,遇污染随时清洁及消毒。
• 护目镜每天用500mg/L含氯消毒液浸泡消毒或用75%酒精擦拭消毒。
• 测温枪用75%酒精每天至少消毒两次,遇污染时随时消毒。
医疗废物处置
1.医疗机构在诊疗新型冠状病毒产生的废弃物,包括医疗废物和生活垃圾,均应当按照医疗废物进行分类收集。
2.包装容器。医疗废物专用包装袋、利器盒的外表面应当有警示标识,在盛装医疗废物前,应当进行认真检查,确保其无破损、无渗漏。医疗废物收集桶应为脚踏式并带盖。医疗废物达到包装袋或者利器盒的3/4时,应当有效封口,确保封口严密。应当使用双层包装袋盛装医疗废物,采用鹅颈结式封口,分层封扎。
3.收集标注。按照医疗废物类别及时分类收集,确保人员安全,控制感染风险。盛装医疗废物的包装袋和利器盒的外表面被
感染性废物污染时,应当增加一层包装袋。分类收集使用后的一次性隔离衣、防护服等物品时,严禁挤压。每个包装袋、利器盒应当系有或粘贴中文标签,标签内容包括:医疗废物产生单位、产生日期、类别、重量,并在特别说明中标注 “新冠”。
4.标本处理。医疗废物中含病原体的标本和相关保存液等高危险废物,应当在产生地点进行压力蒸汽灭菌或者化学消毒处理,然后按照感染性废物收集处理。
对动物疫病检测的启示
一是试剂选择非常关键的,应着重考虑质量稳定、敏感性、特异性三要素。目前我们要求每做一个样品,同时用两种试剂来校对,建议自始至终选择一种可靠、熟悉的试剂,如果频繁更换试剂,可能出现阳性或假阳性问题。
二是样本采集。以前行业中在样本采集方面没引起足够重视,对取样的位置、流程较不规范,一个养殖场户养殖环境中可能存在多种病原,如果样本被污染,会直接影响检测结果,所以对组织、血液、内容物、分泌物的采集应科学规范,只有保证材料的准确性,才能保证检测查的准确性。
三是样本的转运及处理应严格规范。对于人的新冠病毒检测,无论是免疫试纸、血清用来检测抗体的,整个转运过程要求非常严格。如要检测家禽的鼻炎,应采集鸡的鼻拭子,那如果要检测鼻炎的嗜血杆菌,那就不可以反复冻融,可放置甘油中保存运输。
四是仪器设备。新冠病毒检测对仪器设备要求非常严格,需要拥有医疗检测机构的资质。通过做好规定的仪器设备配置,从而保证检测数据的稳定性。
五是要高度重视环境因素。从动物疫病检测方面讲,无论是专业检测实验室还是普通实验室,因为每天需要检测多种病料,可能存在交叉污染。在做新冠病毒检测时,每处理一个样品需要严格消毒,然后再处理下一个样品,这样就避免了环境的交叉污染。除了对实验室的环境要求,对外界环境,包括集装箱,冷藏室、酒店都有环境检测。
六是严格规范操作规程。操作规程非常繁琐复杂,如从样本采集、样本转运、样本保管、核酸提取、PCR操作程序,每一步都有多个规程,需要大家重视并严格落实。
此外,还要重视废弃物处理,前面已讲,此处不赘述。
Copyright © 2012-2026 青岛立见生物科技有限公司版权所有 备案号:鲁ICP备2023002249号-1
 鲁公网安备 37020602000276号
信息公示
鲁公网安备 37020602000276号
信息公示
技术支持:微动力网络