时间:2021-01-18 09:21:36 点击:次
本文纯属个人观点,欢迎交流;
版权所有,征得同意方可转载。
建议点击下载标准全文后再读本文。
国家标准即中华人民共和国国家标准简称国标,是指由国务院标准化行政主管部门或者其他有关主管部门对需要在全国范围内统一的技术要求制定的技术规范。
2020年12月14日国家标准化管理委员会,2020年28号公告正式发布新版《非洲猪瘟诊断技术》国家标准(GB/T 18648-2020),代替GB/T 18648-2002,并于2020年12月14日正式实施。


本标准的范围
本标准规定了非洲猪瘟的临床诊断和实验室诊断方法;临床诊断依据临床症状和病理变化,可初步判定为疑似非洲猪瘟病例,然后进行实验室诊断,对病例作出是否为非洲猪瘟的诊断。本标准适用于家猪和野猪的诊断与监测,并不适用于人、其他动物、植物以及饲料等。
本标准的方法和商品化试剂
1、国标“方法”是根据基础技术和理论进行比较,规定不同方法的检测结果之间的判定优先权,与商品化试剂、仪器设备、工具、人员无关。方法用于“检测”,对临床病例的“确诊”需要综合判定。
2、CNAS认可实验室根据“检测和校准实验室能力认可准则(ISO/IEC 17025:2017)”进行检测,应使用“国际标准、区域标准或国家标准”发布的方法。
3、采用国标方法开发生产的商品化试剂,可称为国标试剂;采用非国标方法或者原理开发生产的商品化试剂,可称为非标试剂。
本标准中方法的分类
本标准中规定的用于非洲猪瘟实验室诊断的“方法”,从检测靶标物质的分子水平上,可以分为三大类,即核酸检测方法、病毒(完整颗粒)检测方法和抗体检测方法。
考虑到生物安全和相关政策要求,本标准不支持病毒分离、培养和鉴定等基础病毒学操作技术作为非洲猪瘟的诊断方法,亦未提供ASFV是否为活病毒、是否具有感染力的检测方法。目前符合相关政策要求和生物安全要求,同时能够满足复养复产需要的方法是投放“哨兵动物”,相当于病毒学中的动物感染实验,检测环境中是否存在具有感染力的活的非洲猪瘟病毒颗粒。
1、核酸检测方法
普通PCR方法、荧光PCR方法和荧光RAA方法,检测靶标非洲猪瘟病毒的遗传物质即脱氧核糖核酸(DNA)的一段序列,可简称为核酸检测(见标准7、8、9)。
本标准中核酸检测方法的检测靶标均为ASFV编码P72蛋白基因即B646L,且均给出了引物、探针等序列,扩增片段位置和长度各不相同,见图1。
那么以检测ASFV其它基因序列为靶标的商品化试剂均为非标试剂。
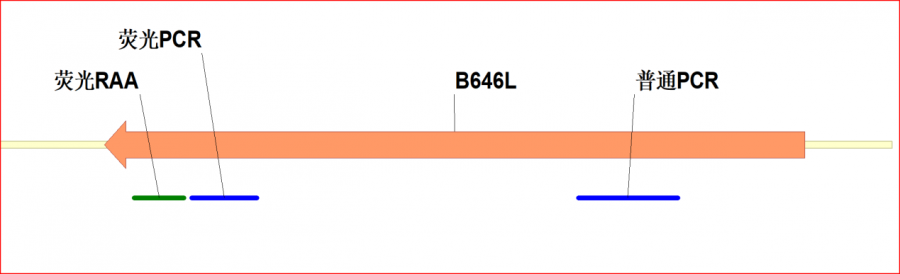
图1 核酸检测方法检测ASFV B646L的长度和相对位置
2、病毒(完整颗粒)检测方法
高敏荧光免疫分析法和夹心ELISA抗原检测法,检测靶标为完整的病毒颗粒,见图2,可简称为病毒(完整颗粒)检测(见标准10、11)。
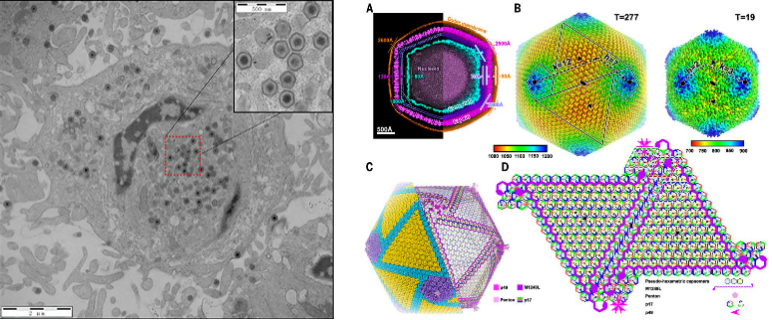
图2 左侧为ASFV病毒超薄切片透射电镜图;右侧为模式图
3、抗体检测方法
间接ELISA抗体检测方法、阻断ELISA抗体检测方法、夹心ELISA抗体检测方法和间接免疫荧光法,检测靶标为猪感染(或免疫)病毒后体内产生的特异性抗体,可简称为抗体检测。
本标准规定的抗体检测方法又可分为全病毒特异性抗体检测方法(见标准15,感染ASFV的细胞)和病毒单一结构蛋白特异性抗体检测方法(见标准12、13、14和15感染重组病毒(表达ASFV蛋白)。
本标准规定的病毒结构蛋白抗体为P54、P30特异性抗体。
本标准方法检测结果判定的等效性和优先权
核酸、病毒(完整颗粒)和抗体三大类方法均可用于实验室诊断,使ASFV的检测国家标准更具有适用性,不同层级的实验室可根据实际条件、检测需求和目的进行选择,同时在综合判定(见标准16)中也依据不同检测方法的最低检出限规定了不同方法检测结果之间的判定优先权和终审权。
核酸和病毒(完整颗粒)检测方法均为阳性具有等效性:核酸检测方法(普通PCR方法、荧光PCR方法、荧光RAA方法)和病毒检测方法(高敏荧光免疫分析法、夹心ELISA抗原检测方法),任何一种方法检测阳性的,可诊断为ASF病例。
核酸和病毒(完整颗粒)检测方法检测结果不同时的判定优先权:当检测结果不一致时,普通PCR方法、高敏荧光免疫分析法和夹心ELISA抗原检测法的任何一种的检测阴性结果,必须服从于荧光PCR方法或荧光RAA方法任何一种阳性结果,可诊断为非洲猪瘟病毒感染。
本项规定,主要是依据不同方法的检测灵敏度确定,见图3、4、5。
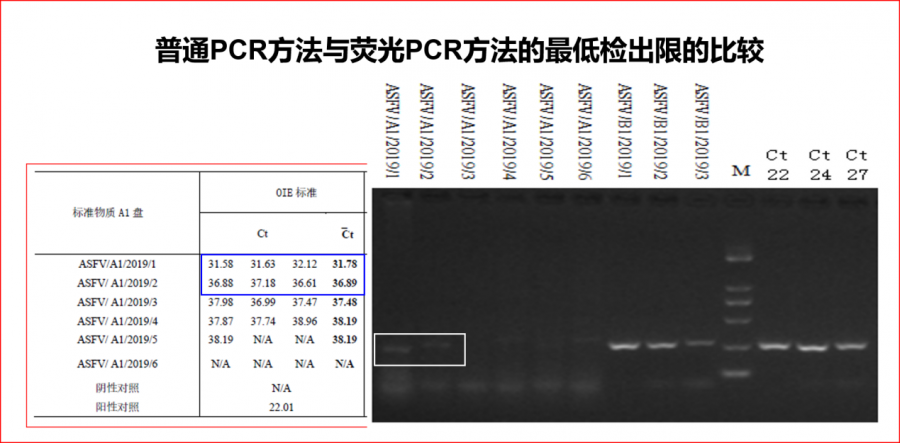
图3 普通PCR与荧光PCR方法最低检出限的比较
荧光PCR检测Ct值为31.78、36.89的样品,用普通PCR方法扩增后,在琼脂糖凝胶电泳中几乎很难看到相应扩增条带。
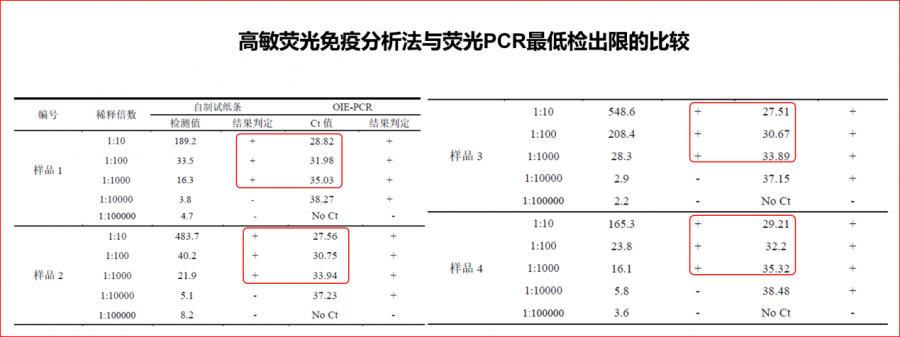
图4 高敏免疫分析法与荧光PCR方法最低检出限的比较
荧光PCR检测Ct值为<35的样品,用高敏免疫分析法,可检测判定为阳性;
荧光PCR检测Ct值为>35的样品,用高敏免疫分析法,可检测判定为阴性。
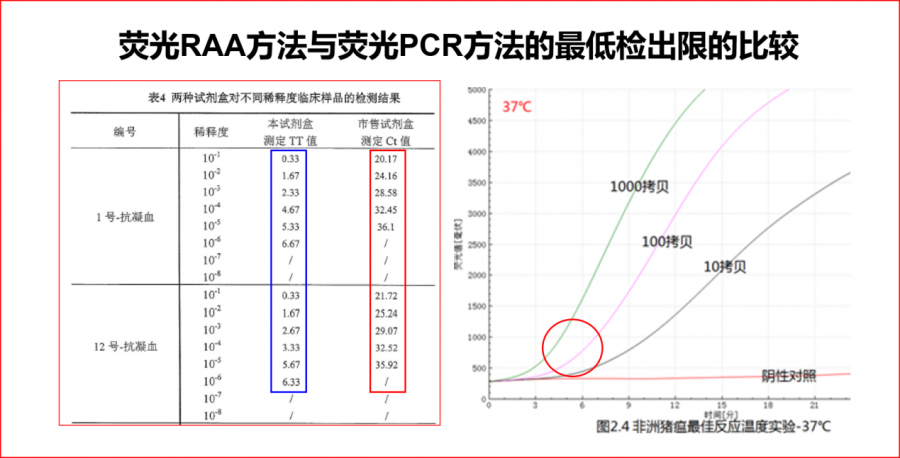
图5 荧光RAA方法与荧光PCR方法最低检出限的比较
荧光RAA方法和荧光PCR方法,在本次实验中检测结果判定几乎一致。
(图3、4、5中的实验数据,受试剂的质量、样品数量和质量、操作、重复次数等因素影响和限制,不能完全反应多种方法最低检出限的相关性)。
抗体检测方法的阳性判定具有等效性:间接ELISA抗体检测方法、阻断ELISA抗体检测方法和夹心ELISA,任一项检测抗体阳性,可诊断为抗体阳性。
ELISA方法检测结果不同时的判定优先权:三种ELISA抗体检测方法的检测结果不一致时,所有检测结果服从间接免疫荧光方法。
(抗体检测不同方法之间相关性的实验数据、图片、敬请期待下一期)
多种方法检测结果判定的等效性和优先权示意图

长按二维码
关注我们

Copyright © 2012-2026 青岛立见生物科技有限公司版权所有 备案号:鲁ICP备2023002249号-1
 鲁公网安备 37020602000276号
信息公示
鲁公网安备 37020602000276号
信息公示
技术支持:微动力网络